Evaluación biológica de 99mTc-Voriconazol como potencial agente de diagnóstico de infecciones fúngicas por centellografía gamma
Laura Reyes, Elena Martinez, Javier Giglio, Mariella Terán.
Resumen / Abstract
Resumen
El avance del HIV ha favorecido el aumento de infecciones fúngicas como candidiasis y aspergilosis invasivas. Varias clases de antifúngicos son utilizados para el tratamiento de las mismas y éstos pueden ser radiomarcados con un agente emisor gamma que permita la detección mediante centellografia de focos de infección. El Voriconazol es un triazol adecuado para la marcación mediante la formación de un complejo unido al precursor [99mTc(H2O)3(CO)3]+. El objetivo fue marcar y determinar las características fisicoquímicas y biológicas del voriconazol con 99mTc para la detección temprana de infecciones. La pureza radioquímica se determinó por HPLC y permitió establecer que el complejo permanece estable durante al menos 120 min. Los estudios in vivo en modelos de inflamación estéril, infección con C. Albicans y A. Niger mostraron diferenciación de los procesos tanto en biodistribución como en imágenes centellográficas.
Agradecimientos: PEDECIBA-Química, OIEA.
Abstract
The spread of HIV has led to an increase of fungal infections such as candidiasis and invasive aspergillosis. Several types of antifungals are used to treat them and some of them can be radiolabeled with a gamma emitting agent to allow detection by scintigraphy of foci of infection. Voriconazole is a triazole agent, suitable for the synthesis of a complex linked with the precursor [99mTc(H2O)3(CO)3]+. The aim of his work was to label and determine the physicochemical and biological characteristics of voriconazole with 99m for the early detection of fungal infections. Radiochemical purity was determined by HPLC and the complex remained stable during at least 120 min. In vivo studies in rats bearing either sterile inflammation, infection with C. Albicans or A. Niger showed differentiation of the processes not only in biosdistribution but also in scintigraphic images.
Acknowledgements: PEDECIBA-Química, IAEA.
Introducción
Las infecciones oportunistas siguen siendo la principal causa de morbimortalidad en los pacientes inmunocomprometidos. La patología infecciosa en pacientes con inmunodepresión avanzada suele ser un problema de difícil resolución, con un claro impacto en la estadía hospitalaria y resultados finales del tratamiento. La poca expresividad clínica de los cuadros infecciosos en este tipo de pacientes hace que su diagnóstico etiológico sea frecuentemente difícil(1-6).
El poder identificar en forma temprana la etiología del cuadro infeccioso redunda en un mejor manejo clinic, aunque con las herramientas diagnósticas disponibles hasta el momento esto permanence como un desafío. Por otra parte, el avance del HIV ha favorecido el aumento de infecciones fúngicas como candidiasis y aspergilosis invasivas. Varias clases de antifúngicos son utilizados para el tratamiento de las mismas y algunos de éstos pueden ser radiomarcados con un agente emisor gamma que permita la detección mediante centellografía de los focos de infección(7-10).
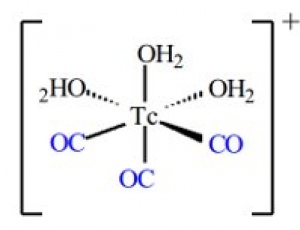
El Voriconazol es un antifúngico de amplio espectro generalmente utilizado para el tratamiento de infecciones invasivas graves en pacientes inmunocomprometidos (fig. 1). Es particularmente adecuado en el tratamiento de aspergilosis invasiva, candidiasis en pacientes no neutropénicos, infecciones invasivas graves por Candida (incluyendo C. Krusei) resistentes a fluconazol y tratamiento de infecciones fúngicas graves por Scedosporium Spp. y Fusarium Spp.(11,12).

Este agente es un triazol adecuado para la marcación uniéndolo a un complejo precursor. El precursor organometálico elegido es el [99mTc(H2O)3(CO)3]+, pues tiene varias ventajas: es fácil de preparar, puede ser usado en muy bajas concentraciones y es viable en agua, solución salina o buffer. Las moléculas de H2O presentes en el mismo son fácilmente sustituibles por un gran número de ligandos{ref 13.14}.
El objetivo del presente trabajo fue el desarrollo y evaluación fisicoquímica y biológica de un potencial radiofármaco para la detección temprana de infecciones fúngicas en pacientes inmunocomprometidos, mediante la formación de complejos tricarbonílicos de 99mTc y Voriconazol.
Método
Formación del precursor [99mTc(H2O)3(CO)3]+
Se incorporan 4 mg de carbonato de sodio (Na2CO3), 7 mg de borohidruro de sodio (NaBH4) y 20 mg de tartrato de sodio y potasio (C4H4O6NaK) en un vial sellado y se purga con CO (g) durante 15 min a presión constante. A esa mezcla se agrega entre 740 a 1110 MBq (20-30 mCi) de pertecneciato (99mTcO4-) en aproximadamente 1 mL de solución salina. Se incuba la preparación en un baño de agua a 70ºC durante 20 min. Una vez finalizado el calentamiento, se neutraliza con buffer fosfato (NaH2PO4) 390 mg/mL en una relación volumen/volumen de (4:1) carbonilo: fosfato. El pH debe ser de 7 al final de la neutralización. La pureza radioquímica del precursor tricarbonílico es controlada por HPLC (fig. 2).
Sistema de HPLC
Columna: Macherey-Nagel C18 5μ 25cm.
Flujo: 1,0 mL/min.
Fase móvil: A- Buffer fosfato trietilamina (2.86mL de H3PO4 por litro) pH: 2,5.
B-Metanol.
Gradiente: 0 a 3 min 100% A.
3 a 6 min de 100% a 75% de A.
6 a 9 min de 75% a 66% de A.
9 a 20 min de 66% a 0% de A.
20 a 27 min 0% de A.
27 a 30 min de 0% a 100% de A.
Sustitución del acuo complejo
La sustitución de las moléculas de agua del precursor por el ligando de interés, en este caso Voriconazol (L): [99mTc(CO)3-L]+, se realiza tomando una alícuota de 250 L del precursor neutralizando al que se le adicionan 550 L de agua y 5 mg de Voriconazol (L) previamente disuelto en 200 L de EtOH. Se incuba en baño de agua a 70º durante 20 minutos. Se controla la pureza radioquímica por HPLC con el mismo sistema antes mencionado.
Estabilidad en el tiempo
Se controla la estabilidad del compuesto tricarbonilo-voriconazol a lo largo del tiempo a 1 y 3 horas post marcado, utilizando el mismo sistema de HPLC.
Estabilidad frente a Histidina o Cisteína
Se determina la estabilidad del compuesto tricarbonilo-voriconazol incubando el mismo conjuntamente con una solución acuosa de histidina (0,8 mg/mL) en baño de agua a 37ºC. El mismo proceso se realiza incubando con una solución de cisteína en idénticas condiciones a las antes mencionadas. Ambos procesos son controlados por HPLC.
Unión a proteínas plasmáticas
Se incuba por triplicado 25 µL del compuesto tricarbonilo-voriconazol con 475 µL de plasma humano en un baño de agua a 37ºC. Se controla la unión a proteínas plasmáticas a 30 y 60 min, tomando 50 µL de la mezcla y sembrando en una mini columna de gel filtración (Sephadex G50). Se centrifuga a 2000 rpm durante 2 min y se mide el número de cuentas obtenido en el eluído y el remanente en la columna.
Unión a levaduras.
Se preparan las soluciones descritas en la Tabla 1. Todas las soluciones y viales deben ser mantenidos en frío (baño de hielo).
| Solución A | Buffer fosfato 14 mM pH 7,5 |
|---|---|
| Suspensión B | Suspensión de C. Albicans de 12 x 108 ufc/mL |
| Solución C | Tween 80 al 0,01% en buffer A (v/v). |
| Solución D | Ácido acético al 0,1 % (v/v). |
| Solución E | Mezclar v/v solución C y D inmediatamente antes de su uso y almacenar a 4ºC. |
Se trabaja con una suspensión de Cándida Albicans (susp. B) en solución A. A partir de ésta se preparan 7 diluciones al medio seriadas de B con solución salina NaCl 0,9% en tubos Eppendorf y un blanco solo con NaCl 0,9%. El volumen final en tubo es 0,4 mL.
A cada tubo se adicionan 0,8 mL de solución E, se incubi 15 min a 4ºC y se agrega a cada uno 0,1 mL de la molécula marcada diluida previamente a 1/10 en buffer A. Se incuba 1 h a 4ºC. Se mide la actividad total a toda la serie. Se centrifuga a 2500 rpm durante 5 minutos a 4ºC, se descarta el sobrenadante, luego se resuspende el pellet en 1 mL de solución E y se vuelve a centrifugar a 2500 rpm durante 5 minutos a 4ºC. Se descarta cuidadosamente el sobrenadante cuidando de no remover el pellet y se mide la actividad final del pellet. Todo el procedimiento se realiza por duplicado.
Modelo animal
Se trabajó con Ratas Wistar hembras de 3 meses, peso 200 ± 20 g. Los modelos de inflamación e infección fueron previamente autorizados por la Comisión Honorara de Experimentación Animal (CHEA 07-05-10) y se detallan en la Tabla 2.
Luego 48 horas de desarrollo de la lesión se inyectó en vena de la cola 2,6 a 5,5 MBq (0,07-0,15mCi) de [99mTc (CO)3-Voriconazol] en los 4 grupos de animales (N=5) y se realizaron biodistribuciones a 1 y 4 horas post inyección a cada animal. Una vez transcurridos los tiempos de biodistribución, se procedió a la disección de los animales, midiendo la actividad presente en los órganos de interés así como también en la muestra de tejido muscular extraído de la pata sana y de la lesionada. También se realizaron imágenes por centellografía gamma de tres ejemplares de animales sanos, con inflamación y con infección.
| Grupo (N=5) | Lesión en pata izquierda trasera | Modo de inducción | Tiempo de desarrollo de lesión |
|---|---|---|---|
| 1 | Inflamación estéril | 100 µL de emulsión al 50% trementina/H20. Vía ip | 48h |
| 2 | Infección C.Albicans | 100 µL suspensión 108 cfu. Via ip | 48 h |
| 3 | Infección A.Niger | 100 µL suspensión 108 cfu. Via ip | 72 h |
| 4 | Control (sanas) | 100 µL NaCl 0,9% estéril. Via ip | 48 h |
Resultados
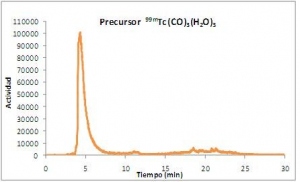
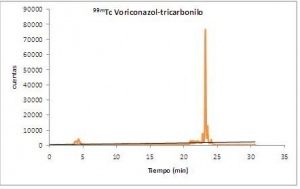
El precursor tricarbonílico presenta una pureza radioquímica promedio de 98%, lo que permite continuar con el proceso de sustitución (fig. 3). Se obtiene el complejo [99mTc(CO)3-Voriconazol] en las condiciones antes mencionadas, con un rendimiento promedio del 90% (fig. 4).
Estudios in vitro
Los estudios de estabilidad en el tiempo demostraron que la sustitución es estable durante al menos 120 min, luego de lo cual se descompone a otras especies. Cuando el complejo se enfrenta a agentes competitivos como Histidina y Cisteína, se descompone entre un 50-75% en un lapso de 60 min. El estudio de unión a proteínas plasmáticas establece que ésta llega al 15%, indicando su disponibilidad para alcanzar el sitio de interés. La unión a levaduras muestra niveles bajos, no superando el 5%.
Estudios in vivo
Los estudios in vivo se realizaron a 1 y 4 horas post administración del radiofármaco; en este trabajo se presentan las gráficas correspondientes a 4 horas, pues resultó el tiempo en que mejor se visualizó la captación en los tejidos de interés. La figura 5 muestra un gráfico comparativo de los porcentajes de actividad por gramo (% Act/g) en tejidos de interés en los modelos animals: sano, inflamación estéril, infección por A.Niger e infección por C.Albicans.
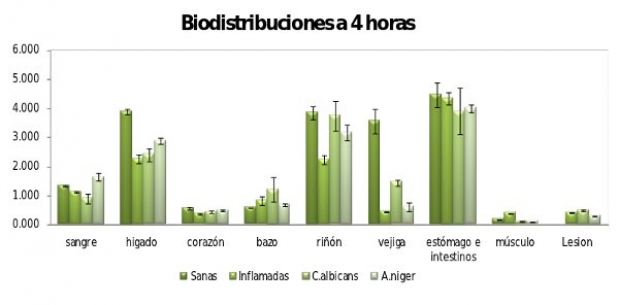
En el grupo de ratas sanas, como es de esperar, se observa una mayor eliminación ya que no existe retención en lesiones. En el caso de ratas con lesions, se observa una menor eliminación por orina mientras que la metabolización hepatobiliar se muestra como la vía preferente. Para evaluar las relaciones de captación entre tejido no blanco o sano (NT: non target) y blanco o lesión (N: target) se realizó el cociente T/NT de los porcentajes de actividad por gramo de muestra (fig. 6).
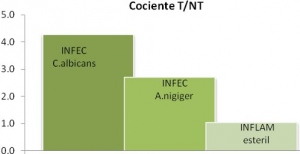
La relación T/NT se presentó claramente diferenciada entre los modelos analizados, siendo: Inflamadas T/NT= 1,20, Infectadas A.Niger T/NT=2,60 e Infectadas C.Albicans T/NT= 4,2. Las imágenes centellográficas muestran las diferencias de captación de acuerdo al tipo de lesión desarrollada. Aunque en las imágenes la diferenciación no es tan clara como en los datos de biodistribución, el modelo infectado con C.Albicans es el que presentó mejor resolución (fig. 7).

Discusión
Fue posible marcar exitosamente el antifúngico voriconazol con una alta pureza radioquímica y estabilidad in vitro. Los estudios in vivo permitieron diferenciar claramente la infección producida por C. Albicans y A. Niger de la inflamación estéril, particularmente en las distribuciones biológicas. Los valores de relación T/NT de inflamación y animales sanos no fueron significativamente diferentes. Las imágenes centellográficas respaldan estos hallazgos preliminaries, mostrándose más claras para la infección con C.Albicans; sin embargo, la alta captación hepática hace que este agente no sea adecuado para lesiones abdominales pues quedarían enmasacaradas. Los estudios preliminares con Voriconazol se perfilan como auspiciosos para el diagnóstico temprano de infecciones por C.Albicans.
Referencias
- Terán.M; Paolino.A; Vilar.J; Kapitan M; Hermida JC, Andruskevicius P, et al. Evaluación clínica y dosimétrica de 99mTc-Hynic-IgG como agente de diagnóstico de focos de infección en pacientes HIV positivos. Rev Panam Infectol 2010;12:12-7.
- Welling A, Lupetti M, Balter H, Lanzzeri S, Souto B, Rey A, et al. 99mTc-labeled antimicrobial peptides for detection of bacterial and Candida albicans infections. J Nucl Med 2001;42,5:788-94.
- Liu S. Bifunctional coupling agents for radiolabeling of biomolecules and target-specific delivery of metallic radionuclides. Adv Drug Deliv Rev 2008;60:1347-70.
- Shaha SQ ullah Khanb M. Radiosynthesis and biological evaluation of the 99mTc-tricarbonyl moxifloxacin dithiocarbamate complex as a potential Staphylococcus aureus infection radiotracer. Appl Radiat Isot 2011;69:686 - 90.
- Kowalski R, Falen S. Radiopharmaceuticals in Nuclear Medicine. 2º Edición. American Pharmacists Association. Washington DC, 2004.
- Signore.A, D´Alessandria A, Lazzeri.A, Dierckx R. Can we produce an image of bacteria with radiopharmaceuticals? EurJ Med Mol Imaging 2008;35:1051-5.
- Lupetti M, Welling A, Mazzi U, Nibbering P, Pauwels E. Technetium-99m labelled fluconazole and antimicrobial peptides for imaging of Candida albicans. J Nucl Biol Med 2002;29:674-9.
- Alberto R, Schibili R, Egli A, Schubiger AP. A novel organometallic aqua complex of technetium for the labeling of biomolecules: Synthesis of [99mTc(OH2)3(CO)3]+ from [99mTcO4]- in aqueous solution and Its reaction with a bifunctional ligand. J Am Chem Soc 1998;120:7987-8.
- Lupetti A, Welling MM, Pauwels EK, Nibbering PH. Detection of fungal infections using radiolabeled antifungal agents. Curr Drug Targets 2005;6:945-54.
- Carlo P, Brouwer WM, Welling A. The pharmacology of radiolabeled cationic antimicrobial peptides. J.Pharm Sci 2008;97:1633–51.
- Alberto R, Schibili R, Waibel R, Abram U, Schubiger AP. Basic aqueous chemistry of [M(OH2)3(CO)3]+ (M= Re, Tc) directed towards radiopharmaceutical application. Coordination Chemistry Reviews 1999;190-192:901-19.
- Schibili R, Schubiger PA. Current use and future potential of organometallic radiopharmaceuticals. Eur J Nucl Med Mol Imaging 2002;29:1529-42.
- Kuijpers B, Groothuys S, Keereweer A. Synthesis of Triazole-linked glicosyl amino acids and peptides. Org Lett 2004;6:3123-6.
- Tokita N, Hasegawa S, Maruyama K, Izumi T, Blankenberg FG, Tait JF, et al. Use of radiolabelled peptides for scintigraphy in non-oncologic diseases. 99mTc-Antimicrobial peptides: promising candidates for infection imaging. Q J Nucl Med 2003;47:238-45.
