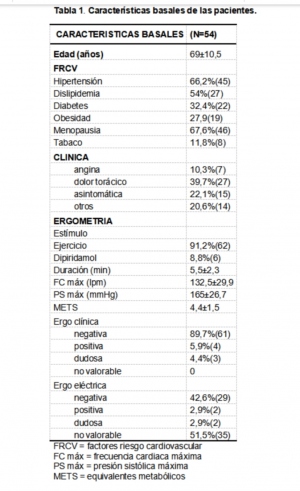
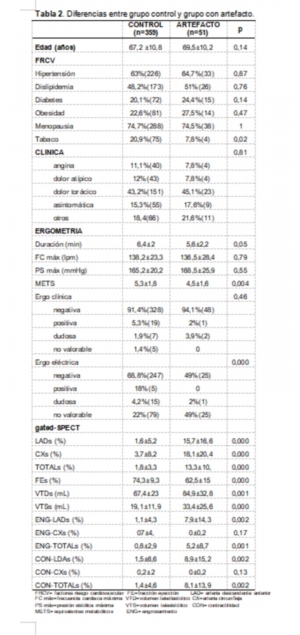
Artefacto por atenuación mamaria en Gated-SPECT de mujeres con probabilidad pre-test baja o intermedia de cardiopatía isquémica
Berta Covadonga Lorente Castro1, Pablo Jané Soler1, Isabel López Villar1, Alberto Martínez Lorca1, Juan Antonio Pérez Iruela1, María del Val Gómez Martínez1.1 - Servicio de Medicina Nuclear, Hospital Universitario Ramón y Cajal. Madrid, España..
Resumen
Objetivo: Demostrar el significado del artefacto por atenuación mamaria en mujeres con probabilidad pre-test baja/intermedia que acuden a Medicina Nuclear por sospecha de cardiopatía isquémica (CI).
Método: Se estudiaron 54 pacientes mujeres con probabilidad pretest baja/intermedia de CI y defectos de atenuación atribuidos a artefacto por atenuación durante 46 ± 10,2 meses.
Resultados: En 19 el defecto fue en cara anterior, en 18 ánterolateral y en 14 lateral. Se realizó coronariografía a 19; en 3 aparecieron lesiones significativas. Se comparó a las 51 sin evidencia de CI con un grupo control. No hubo diferencias significativas en las características basales, contractilidad y engrosamiento parietal. Ninguna presentó eventos cardiovasculares mayores.
Conclusiones: La aparición de defectos de perfusión en cara anterior o lateral por artefactos por atenuación mamaria es relativamente frecuente. Éstos no se acompañan de alteraciones del engrosamiento y la motilidad. Para una adecuada interpretación son indispensables la clínica y la ergometría.
Palabras clave: cardiopatía isquémica, mujeres, gated-Spect, artefacto por atenuación mamaria
Abstract
Objective: To establish the significance of breast attenuation in women with low/intermediate pre test probability referred to Nuclear Medicine for suspected ischemic heart disease (IHD).
Method: Fifty-four women with a low/intermediate pre test probability presenting with perfusion defects attributed to breast attenuation were studied for 46±10.2 months.
Results: In 19 the defect was anterior, in 18 anterolateral and in 14 lateral. Catheterization was performed in 19; significant lesions were found in 3. The 51 patients with no evidence of IHD were compared with a control group. No significant differences were observed in baseline characteristics, wall motion and thickening. During the follow-up period, no major cardiovascular events occurred.
Conclusions: The observation of perfusion defects in the anterior or lateral left ventricular walls by breast attenuation is relatively frequent. These are not associated with alterations of wall motion and thickening. For a correct interpretation of the results, clinical and electrocardiographic correlation is crucial.
Key words: ischemic heart disease, women, gated-Spect, breast attenuation artifact
Introducción
La gammagrafía de perfusión miocárdica es un método ampliamente aceptado, no invasivo y coste efectivo para el diagnóstico y la evaluación pronóstica de la cardiopatía isquémica (CI)(1,2). Sin embargo, una de las mayores limitaciones a la especificidad de la exploración es la atenuación de los fotones por los tejidos blandos, que se traduce en resultados falsamente positivos. En los hombres, la causa más frecuente de atenuación son los órganos infra-diafragmáticos que originan defectos en la cara inferior, mientras que en las mujeres se producen sobre todo defectos en las caras anterior y lateral del ventrículo izquierdo (VI) como consecuencia de la atenuación mamaria(3,4). Estos artefactos son más prominentes en mujeres con mamas voluminosas o densas(1,5). Esta dificultad para el diagnóstico se suma a otras características de la CI en la mujer, como la presentación clínica atípica o el diferente perfil de los factores de riesgo cardiovascular (FRCV), todo lo cual suele conducir a un sesgo de género en el manejo de la enfermedad(6).
El uso del tecnecio-99 metaestable (99mTc) para el estudio de la perfusión miocárdica, cuyas características físicas lo hacen particularmente adecuado para la obtención de imágenes, ha reducido de forma sustancial el problema de atenuación por tejidos blandos en comparación con el talio-201 (201Tl)(7). Sin embargo, este tipo de artefactos aún representa un problema para la correcta interpretación de la SPECT en mujeres(8,9) y la experiencia del operador se torna un factor esencial para su reconocimiento. El propósito del presente trabajo ha sido mostrar nuestra experiencia en la interpretación de los defectos de perfusión que aparecen en mujeres con sospecha de CI y probabilidad pre-test intermedia/baja que pueden atribuirse a atenuación mamaria y describir las características de la población que presentó este fenómeno.
Método
Pacientes
Para la presente investigación se utilizó una muestra de datos de la población que componían el estudio observacional titulado: “Registro de Pacientes con Exploraciones de Medicina Nuclear de las Áreas Cardiopulmonar y Vascular” aprobado por el comité de ética de nuestro hospital. Se recogieron de forma consecutiva los datos de 441 pacientes del sexo femenino que acudieron al servicio de Medicina Nuclear entre abril de 20013 y octubre 2016 para evaluación de isquemia miocárdica. Se consideraron 54 (12,24%) pacientes que cumplieron los criterios de inclusión: baja/intermedia probabilidad pre-test para CI(10) y defectos de perfusión de al menos 10%(11) en la cara anterior y/o lateral del VI en el estudio en estrés. Las pacientes fueron seguidas evolutivamente durante un tiempo medio de 46 ± 10,3 meses, teniendo en cuenta la información clínica, el resultado de otras exploraciones complementarias y la aparición de eventos coronarios. Los resultados fueron comparados con los obtenidos de una base de datos formada por 359 mujeres con estudios de perfusión miocárdica que presentaban un resultado normal. La probabilidad pre-test se estableció de acuerdo a las directrices actuales de la Sociedad Europea de Cardiología (SEC) según el sexo, la categoría de edad y el tipo de angina de pecho (típica, atípica o dolor no anginoso)(12) así como según los criterios de Diamond y Forrester(10). Los criterios de exclusión fueron tener historia de CI, cardiomiopatía (tanto hipertrófica como dilatada), o bloqueo completo de rama izquierda (BCRI) del haz de His. Los eventos cardiovasculares mayores considerados durante el periodo de seguimiento fueron el infarto agudo de miocardio (IAM) y la muerte de origen cardíaco. En todos los casos se contaba con una encuesta estructurada en las que se reflejaban su edad, antecedentes personales, FRCV, clínica, tratamiento recibido, comorbilidades sistémicas y cardiovasculares y ECG basal.
Prueba de estrés
Se realizó prueba ergométrica mediante ejercicio sobre tapiz rodante siguiendo el protocolo de Bruce, o Bruce modificado en rampa. Se consideró la clase funcional, la capacidad funcional en equivalentes metabólicos (METs) y se consignó la respuesta clínica (dolor torácico) y eléctrica. La respuesta positiva del ECG se definió como una depresión horizontal o descendente del segmento ST ≥1 mm a 80 ms después del punto J, o una elevación del ST ≥1 mm, que se hayan producido durante el ejercicio o hasta 2 minutos en la recuperación(13).
Estudio de perfusión miocárdica (gated-SPECT)
Se realizó gated-SPECT sincronizando la adquisición de las imágenes con el ECG. El radiofármaco utilizado fue 6-metoxi-isobutil-isonitrilo (MIBI) marcado con 99mTc en dosis de 555 MBq tanto para el estrés como para el reposo, en protocolo de un día. En casos en que el estudio de estrés fue normal, no se obtuvo la fase de reposo. Las imágenes fueron adquiridas después de 30 minutos de la administración del radiotrazador, mediante una gamma cámara de doble cabezal (Infinia-Hawkeye, GE) dispuesto a 90°, equipada con colimadores de alta resolución, baja energía y orificios paralelos (LEHR). Se obtuvieron 62 imágenes en arco de 180° con órbita elíptica desde la posición oblicua anterior derecha hasta la oblicua posterior izquierda, con la paciente en posición supina. La reconstrucción de datos se realizó mediante software dedicado (4D-MSPECT, University of Michigan, USA) obteniéndose imágenes tomográficas de perfusión y datos cuantitativos a partir de mapas polares. Los defectos de perfusión en las imágenes de estrés y en su caso en las de reposo se expresaron en forma de porcentaje de miocardio afectado respecto al miocardio total, o bien en cada territorio coronario por separado, a saber: arteria descendente anterior (DA), circunfleja (Cx) y coronaria derecha (CD). Los defectos de perfusión se clasificaron de forma semicuantitativa en: pequeños o no significativos (extensión ≤9%) y en significativos, con extensión ≥10% (dentro de los cuales el defecto moderado se consideró entre 10% y 20% y el severo como >20% del total del VI)(10). Según sus características y tras la realización del estudio en situación de reposo, los defectos de perfusión se clasificaron como fijos, reversibles o parcialmente reversibles. Se cuantificó la función global del VI mediante la fracción de eyección (FEVI) y los volúmenes telediastólico (VTD) y telesistólico (VTS), así como la función regional mediante el análisis del engrosamiento y la motilidad parietal. Se tomó como límite inferior normal para la FEVI un valor de 50%.(14,15).
Análisis estadístico
Se utilizó el paquete informático SPSS (IBM SPSS Statistics Version 23.0. Armonk, NY, USA). La descripción de la población en cuanto a sus características socio-demográficas y clínicas se llevó a cabo a través de estadísticas descriptivas (proporciones y medidas de centralización, media y desviación típica). El análisis de las variables continuas se efectuó mediante el test t de Student, el análisis de proporciones/porcentajes mediante la prueba Chi-cuadrado y la comparación de variables cuantitativas entre los diferentes grupos de estudio mediante la prueba ANOVA. Se consideró una significación estadística p<0,05 en todos los tests.
Resultados
Pacientes con defectos sugestivos de atenuación mamaria
La prevalencia de defectos de perfusión atribuibles a atenuación mamaria por las características clínicas de las pacientes y de la imagen que hallamos en nuestro estudio fue de un 12,24% (54/441) dentro del grupo de mujeres que acudieron a realizarse una prueba por sospecha de CI. De estas 54 pacientes, se realizó coronariografía a 19 (35%); en 3 de ellas (5,5%) se demostraron lesiones significativas (2 con lesión severa en la CD y 1 en la DA proximal). Estas pacientes presentaron defectos de perfusión en el estudio de estrés: defecto leve en la cara anterior (1 caso), moderado en las caras anterior y lateral (1 caso) y severo en la cara lateral (1 caso). Se realizó estudio de reposo en las 3; en 2 de ellas el defecto fue fijo y en una parcialmente reversible. Las características basales de este grupo con defectos sugestivos de atenuación mamaria se presentan en la tabla 1; a modo de ejemplo, se presenta un caso ilustrativo en las figs. 1 y 2.
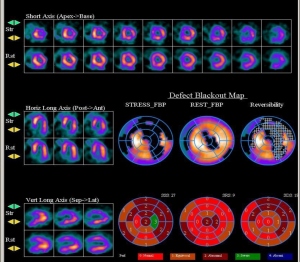
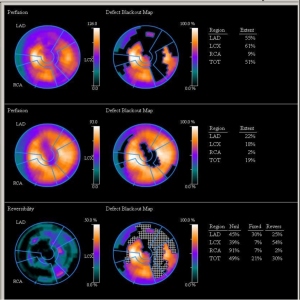
Comparación entre el grupo con artefactos de atenuación sin CI y el grupo control
Se consideró que las 51 pacientes restantes (94%) no presentaban CI, bien por presentar una coronariografía normal (16 pacientes) o por sus datos evolutivos: ausencia de eventos cardiovasculares mayores, ausencia de sintomatología clínica de CI y situación de alta en las consultas de cardiología. Comparando las características basales de las 51 mujeres en las que se encontró un defecto de perfusión interpretado como artefacto de atenuación con el grupo de 359 pacientes con perfusión normal, observamos que la edad es mayor en las primeras (69,57 ± 10 vs 67,5 ± 11 años), la sintomatología más frecuente fue dolor torácico en ambos grupos (45% vs 43%); la prevalencia de hipertensión (65% vs 63%), dislipidemia (51% vs 48%) y obesidad (27% vs 22%) fue similar, mientras que el porcentaje de pacientes diabéticas resultó ser algo mayor (29% vs 20%) y el de fumadoras menor (8% vs 21%).
En cuanto a la ergometría, el resultado fue predominantemente negativo en ambos grupos en cuanto a la presencia de dolor torácico (94% vs 91%), mientras que la negatividad de la prueba eléctrica fue de 69% y 49%, respectivamente. Dentro de los parámetros ergométricos, la duración de la prueba fue menor en el grupo estudiado (5,6 ± 2 vs 6,4 ± 2 minutos) aunque sin valor significativo. La FC máxima fue similar en ambos grupos (136,5 ± 28,4 vs 138,2 ± 23,3 lpm), al igual que el porcentaje máximo de la FC alcanzado (89,5 ± 15,7% vs 89,3 ± 14,4%) y la PAS máxima (168,5 ± 26 vs 165,2 ± 20,2 mmHg); sin embargo los METS fueron menores (4,5 ± 1,6 vs 5,3 ± 1,8).
En lo que refiere a la extensión de los defectos de perfusión expresado en porcentaje, las pacientes en las que se diagnosticó artefacto por atenuación mamaria presentaron diferencias estadísticamente significativas frente al grupo control en las imágenes de estrés, tanto en el territorio de la DA (15,7 ± 16,6% vs 1,6 ± 5,2%; p=0,000) como en el miocardio total (13,3 ± 10,3% vs 1,8 ± 3,3%; p=0,000).
En cuanto a los resultados de la función ventricular global, en el grupo de las 51 mujeres con artefactos por atenuación mamaria, la FEVI post estrés mostró valor más bajo que la del grupo control (62,5 ± 15% vs 74 ± 9%, p=0,000) y el volumen telediastólico (84,9 ± 32,8 ml vs 67,4 ± 23 ml, p=0,001) y telesistólico (33,4 ± 25,6 ml vs 19,1 ± 11,9 ml, p=0,000) fueron mayores que los del grupo control. Los resultados de la comparación de ambos grupos se encuentran reflejados en la tabla 2. Si tenemos en cuenta la función regional, hubo diferencias significativas entre ambos grupos de pacientes, tanto en cuanto al engrosamiento a la motilidad parietal en situación de estrés en el territorio de la DA (defecto de engrosamiento: 14 ± 7,9,3% vs 4,3 ± 1,1%; p=0,002 y defecto de motilidad: 15,2 ± 8,9% vs 6,6 ± 1,5%; p=0,002) y en el defecto total (defecto de engrosamiento: 5,2±8,7% vs 0,8±2,9%; p=0,001 y defecto de motilidad: 8,1±13,9% vs 1,4±4,6%; p=0,002).
Defectos de perfusión en las pacientes con artefacto de atenuación sin CI
La topografía del defecto por atenuación en las mujeres sin CI fue la siguiente: en 19/51 pacientes (37,2%) se localizó en la cara anterior, en 14/51 (27,4%) en la cara lateral y en 18 /51 (35,2%) en la cara ánterolateral. Se obtuvieron imágenes de reposo en 31/51 pacientes (60%) a fin de comprobar la reversibilidad; se observó un defecto reversible en 15/31 (48,3%), de los cuales parcialmente reversible en 10/15 (66,6%) y totalmente reversible en 5/15 (33,3%), y un defecto fijo en 16/31 mujeres (55,6%).
De las 19 pacientes (37,2%) que presentaron defecto en la cara anterior, 14/19 (73,6%) tuvieron engrosamiento parietal normal, 13/19 (68,4%) motilidad normal y 11/19 (57,8%) mostraron engrosamiento y motilidad normales. Hubo 14 pacientes (27,4%) con defecto en la cara lateral, de las cuales 12/14 (85,7%) tuvieron engrosamiento normal, 13/14 (92,8%) motilidad normal y 12/14 (85,7%) mostraron engrosamiento y motilidad normales. En las 18 pacientes (35,2%) con defecto en cara ánterolateral, 11/18 (61,1%) tuvieron engrosamiento normal, 11/18 (61,1%) presentaron motilidad normal y 9/18 (50%) engrosamiento y motilidad normales (tabla 3).
Seguimiento evolutivo del grupo con artefacto por atenuación mamaria
Durante el tiempo de seguimiento, ninguna de las 54 pacientes con defectos interpretados como atenuación presentaron eventos cardiovasculares mayores, aunque hubo 24 (44,4%) que tuvieron episodios de dolor torácico, que no requirieron intervención.
Discusión
Son conocidas las diferencias de género que existen en relación a los síntomas clínicos de CI; las mujeres exhiben con mayor frecuencia síntomas atípicos como disnea, náuseas, mareo, reflujo, dispepsia, incluso diaforesis, y además presentan mayor edad, todo lo cual afecta al diagnóstico y al tratamiento de la enfermedad coronaria(16,17). Las dos causas principales que disminuyen la especificidad de la prueba de perfusión miocárdica en mujeres parecen ser el tamaño usualmente más pequeño del corazón y los efectos altamente variables de la atenuación de la mama. La atenuación mamaria en los estudios de gated-SPECT ha sido tratada quizás algo menos de lo que se debería en la literatura médica. Han sido, por ejemplo, autores como Fícaro(18,19) Hendel(20,21) o Fessler(22,23) algunos de los grandes impulsores de este tema, ya que se trata de un hallazgo relativamente frecuente en la práctica clínica. Así, en nuestro estudio ha aparecido en un 12,24% de las mujeres con probabilidad pre-test intermedia/baja que acudieron a nuestro servicio por sospecha de CI. Para autores como Hansen et al.(4), los artefactos por atenuación mamaria producen un patrón de disminución de la captación en la cara anterior, con una preservación relativa en el ápex. Sin embargo, en nuestro estudio los defectos de perfusión atribuidos a atenuación mamaria han aparecido no solo en la cara anterior sino también en las caras anterolateral y lateral, afectando los territorios irrigados por las arterias DA y Cx.
Los artefactos relacionados con atenuación por partes blandas aparecieron en nuestro caso utilizando el software Corridor 4DM, que presenta alta exactitud y buena reproducibilidad de los resultados, aunque también se encuentra descrita la aparición de dichos artefactos con la utilización de otros programas informáticos(24). Las mujeres que presentan artefacto de atenuación mamaria son pacientes con características basales muy similares a la población sin ellos, pero se diferencian por la edad algo mayor y por presentar una FEVI algo menor, con volúmenes ventriculares mayores.
Se han propuesto varios métodos para disminuir los artefactos por atenuación en los estudios de perfusión miocárdica; el más ampliamente aceptado es la corrección de la atenuación mediante una fuente externa (ya caído en desuso) o mediante la realización de una TC de baja dosis; la obtención de imágenes en posición prona también resulta una adecuada opción. Mediante el uso de gamma cámaras con detectores de cadmio-zinc-telurio se han obtenido mejores resultados que con las cámaras convencionales(25). Cada uno de estos métodos presenta sus ventajas e inconvenientes; en general, la corrección de atenuación mejora la especificidad pero disminuye la sensibilidad, sobre todo en el caso de defectos inferiores correspondientes al territorio de la arteria CD(26). La obtención de imágenes en prono no incrementa la dosimetría del paciente, pero aumenta el tiempo de exploración y algunos autores sostienen que es menos eficiente respecto a la aplicación de la corrección de atenuación(27). Por otra parte, hay que tener en cuenta que las nuevas cámaras con detectores de cadmio-zinc-telurio aún no se encuentran disponibles en la mayoría de los centros sanitarios, por lo que en la práctica clínica habitual el diagnóstico de atenuación mamaria se realiza sobre todo en base a la experiencia que el médico nuclear posea en este aspecto.
El reconocimiento del artefacto por atenuación mamaria requiere de una adecuada valoración clínica de la paciente. En nuestro estudio, se pone de manifiesto que tan solo 3 de las pacientes estudiadas dentro del grupo de 54 mujeres con baja probabilidad pre-test y con hallazgo de defectos en cara anterior, lateral o ánterolateral, presentaron lesiones coronarias significativas. Ninguna de las pacientes que presentaron este artefacto tuvo una ergometría eléctricamente positiva, siendo clínicamente anormal en un porcentaje muy bajo (2%), datos que indican el gran auxilio que representa una prueba de esfuerzo negativa para orientar el diagnóstico de artefactos.
En cuanto al pronóstico de las pacientes con defectos de perfusión en las caras anterior y lateral que se interpretaron como atenuación mamaria, el mismo es muy favorable ya que sólo en 3 de ellas aparecieron eventos cardiovasculares mayores durante el seguimiento. El hecho de que los defectos de perfusión fijos se acompañen de motilidad y engrosamiento parietal normales(28), ayuda a distinguir los artefactos por atenuación mamaria de los defectos por necrosis. Los resultados de nuestro estudio apuntan a que los defectos en cara anterior y lateral en mujeres con probabilidad pre-test baja/intermedia de CI que se acompañan de motilidad normal pueden interpretarse como artefactos de atenuación mamaria, siempre que la historia clínica sea concordante y la ergometría sea negativa para isquemia miocárdica.
Limitaciones
La principal limitación del estudio está referida al tamaño de la muestra. En efecto, el número de pacientes es pequeño, ya que entre las 441 pacientes analizadas sólo hallamos 54 que presentaron defectos atribuibles a artefactos de atenuación mamaria en la gated-SPECT. También fueron muy pocas las mujeres a las que se les realizó coronariografía, pero esta decisión del clínico fue concordante con la baja probabilidad de CI y la ausencia de resultados de alto riesgo en las pruebas funcionales. Sin embargo, la falta de pruebas invasivas hace que no contemos con una validación anatómica de nuestros resultados.
Conclusiones
La aparición de defectos de perfusión atribuibles a artefactos por atenuación mamaria es relativamente frecuente en mujeres que acuden para diagnóstico o evaluación de CI. Las características basales de las pacientes que presentan artefactos de atenuación son indistinguibles de la población sin defectos en las pruebas de imagen. Los defectos por atenuación que se localizaron en la cara anterior, lateral y ánterolateral en general no se acompañaron de alteraciones en el engrosamiento y la motilidad parietal. Solamente 3 de 54 mujeres con probabilidad pre-test baja o intermedia de CI y defectos de perfusión en estas regiones presentaron lesiones en la coronariografía.
Los artefactos por atenuación mamaria suelen aparecer con más frecuencia en pacientes de mayor edad y con FEVI relativamente más baja (aunque dentro de lo normal) respecto a pacientes sin este defecto. Durante el periodo de seguimiento de las pacientes con artefacto por atenuación no se registró ningún evento mayor, independientemente de la localización, tamaño o grado de reversibilidad del defecto.
Las dificultades en diagnosticar CI en la mujer y la necesidad de reconocer un artefacto de atenuación, inducen a tener especial cuidado en la interpretación del estudio. Es importante por tanto identificar aquellos subgrupos específicos de pacientes en los cuales la gated-SPECT ofrece un valor incremental en el diagnóstico y pronóstico(28,29). El reconocimiento de este artefacto en mujeres es fundamental para evitar cateterismos innecesarios. Para una adecuada interpretación de los defectos de perfusión producidos por atenuación mamaria es indispensable la correlación con la clínica, así como con el resultado de la ergometría.
Agradecimientos
Debo y tengo el honor de agradecer a mi directora de tesis Dra. María Julia Buján Varela y a la Universidad de Alcalá de Henares, que me proporcionaron el marco adecuado para llevar a cabo una investigación de la cual han dado su fruto dos artículos propios y espero que otros más en el tiempo venidero.
Referencias
- Judelson DR. Examining the gender bias in evaluating coronary disease in women. Medscape Womens Health 1997; 2:5.
- Hung J, Chaitman BR, Lam J, et al. Noninvasive diagnostic test choices for the evaluation of coronary artery disease in women: a multivariate comparison of cardiac fluoroscopy, exercise electrocardiography and exercise thallium myocardial perfusion scintigraphy. J Am Coll Cardiol 1984; 4:8-16.
- Stinis CT, Lizotte PE, Movahed M-R. Impaired myocardial SPECT imaging secondary to silicon- and saline-containing breast implants. Int J Cardiovasc Imaging 2006; 22:449-55.
- Hansen CL, Sundaram S. The ratio of the apex/anterior wall: A marker of breast attenuation artifact in women: Nucl Med Commun 2006; 27:803-6.
- Goodgold HM, Rehder JG, Samuels LD, Chaitman BR. Improved interpretation of exercise Tl-201 myocardial perfusion scintigraphy in women: characterization of breast attenuation artifacts. Radiology 1987; 165:361-6.
- Acevedo M, Varleta P. Exámenes diagnósticos cardiovasculares: ¿diferencias de género en su interpretación? Rev Colomb Cardiol 2018; 25:66-72.
- Taillefer R, DePuey EG, Udelson JE, et al. Comparative diagnostic accuracy of Tl-201 and Tc-99m sestamibi SPECT imaging (perfusion and ECG-gated SPECT) in detecting coronary artery disease in women. J Am Coll Cardiol 1997; 29:69-77.
- Botvinick EH. Breast attenuation artifacts in Tl-201 scintigraphy. Radiology 1988; 168:878-9.
- Garver PR, Wasnich RD, Shibuya AM, Yeh F. Appearance of breast attenuation artifacts with thallium myocardial SPECT imaging. Clin Nucl Med1985; 10:694-6.
- Diamond GA, Forrester JS. Analysis of probability as an aid in the clinical diagnosis of coronary-artery disease. N Engl J Med 1979; 300:1350-8.
- Holly TA, Abbott BG, Al-Mallah M, et al. Single photon-emission computed tomography. J Nucl Cardiol Off Publ Am Soc Nucl Cardiol 2010; 17:941-73.
- Task Force Members, Montalescot G, Sechtem U, Achenbach S, et al. 2013 ESC guidelines on the management of stable coronary artery disease: the Task Force on the management of stable coronary artery disease of the European Society of Cardiology. Eur Heart J 2013; 34:2949-3003.
- Arósa F, Boraita A, Alegría E, et al. Guías de práctica clínica de la Sociedad Española de Cardiología en pruebas de esfuerzo. Rev Esp Cardiol 2000; 53:1063-94.
- Alexiou S, Georgoulias P, Angelidis G, et al. Myocardial perfusion and left ventricular quantitative parameters obtained using gated myocardial SPECT: Comparison of three software packages. J Nucl Cardiol Off Publ Am Soc Nucl Cardiol 2018; 25:911-24.
- Romero-Farina G, Candell-Riera J, Aguadé-Bruix S, et al. Predictive variables for hard cardiac events and coronary revascularization in patients with normal left ventricular myocardial perfusion and systolic function. Eur J Nucl Med Mol Imaging 2013; 40:1181-9.
- Wenger NK. Clinical presentation of CAD and myocardial ischemia in women. J Nucl Cardiol Off Publ Am Soc Nucl Cardiol 2016; 23:976-85.
- Sörensen NA, Neumann JT, Ojeda F, et al. Relations of sex to diagnosis and outcomes in acute coronary syndrome. J Am Heart Assoc 2018; 7:e007297.
- Hendel R, Ficaro E, Williams K. Timeliness of reporting results of nuclear cardiology procedures. J Nucl Cardiol 2007; 14:266.
- Corbett JR, Kritzman JN, Ficaro EP. Attenuation correction for single photon emission computed tomography myocardial perfusion imaging. Curr Cardiol Rep 2004; 6:32-40.
- Hendel RC, Cerqueira M, Douglas PS, et al. A Multicenter assessment of the use of single-photon emission computed tomography myocardial perfusion imaging with appropriateness criteria. J Am Coll Cardiol 2010; 55:156-62.
- Hendel RC, Abbott BG, Bateman TM, et al. The role of radionuclide myocardial perfusion imaging for asymptomatic individuals. J Nucl Cardiol Off Publ Am Soc Nucl Cardiol 2011; 18:3-15.
- Ficaro EP, Fessler JA, Ackermann RJ, et al. Simultaneous transmission-emission Thallium 201 cardiac SPECT: Effect of attenuation correction on myocardial tracer distribution. J Nucl Med 1995; 36:921-31.
- Joonki Noh, Fessler JA, Kinahan PE. Statistical sinogram restoration in dual-energy CT for PET attenuation correction. IEEE Trans Med Imaging 2009; 28:1688-702.
- Malek H, Yaghoobi N, Hedayati R. Artifacts in quantitative analysis of myocardial perfusion SPECT using Cedars-Sinai QPS software. J Nucl Cardiol Off Publ Am Soc Nucl Cardiol 2017; 24:534-42.
- Liu C-J, Cheng J-S, Chen Y-C, et al. A performance comparison of novel cadmium–zinc–telluride camera and conventional SPECT/CT using anthropomorphic torso phantom and water bags to simulate soft tissue and breast attenuation. Ann Nucl Med 2015; 29:342-50.
- Sharma P, Patel CD, Karunanithi S, et al. Comparative accuracy of CT attenuation-corrected and non–attenuation-corrected SPECT myocardial perfusion imaging: Clin Nucl Med 2012; 37:332-8.
- Gutstein A, Bental T, Solodky A, et al. Prognosis of stress-only SPECT myocardial perfusion imaging with prone imaging. J Nucl Cardiol 2018; 25:809-16.
- DePuey EG, Rozanski A. Using gated Technetium-99m-Sestamibi SPECT to characterize fixed myocardial defects as infarct or artifact. J Nucl Med 1995; 36:952-5.
- Chatziioannou SN. Gating of myocardial perfusion imaging for the identification of artifacts. Tex Heart Inst J 2000; 27:5.